无论是号召召回,还是激愤,大家最关心的问题其实是◆◆◆■:诸如超声炮之类的械二超声产品还能用吗?
由于第二类由省级药监部门监管,不同省份可能在管理办法方面有所差异。此次★◆◆◆“超声风波”中所涉及变更的企业,均是拿的第二类医疗器械证,均来自湖南省,据了解,是因为湖南省在这类超声产品注册审批上“比较激进”。
随着行业近年向轻医美的转向,医美声光电类治疗方式快速发展★◆★★★◆,市场规模不断扩容。据高禾投资研究中心预测,我国声光电类医美消费市场规模将于2025年达到508■★◆■.12亿元。医美声光电包含三类:超声类(声)■◆★■■、光学类(光)和射频类(电)◆★◆◆。其中超声技术应用于医美行业较为晚近。
2023年11月23日■◆,国家药监局发布《美容用途超声器械分类界定指导原则(征求意见稿)》,将用于脂肪、胶原蛋白增生和再生◆★◆◆★、痤疮◆■◆◆、色斑、疤痕★■■◆、皮肤弹性★★、皱纹等治疗的超声器械,按照三类械管理。将不发生组织变性★■■■■★,促进皮肤血液循环、加快皮肤新陈代谢的超声器械,和将药械经皮肤或黏膜透入人体的超声美容器械,按照二类械管理。
500)this★◆★◆■◆.width=500 align=center hspace=10 vspace=10 rel=nofollow/
2021年6月,半岛医疗超声炮获批第二类医疗器械证◆◆★★,成为国内医美行业首个获证的超声类医疗设备,也因此一炮而红。它的走红■◆,很大程度上来自于超声刀在国内市场教育先行的市场现状★◆■■◆■,以及国内消费者对医美超声技术的巨大需求。
500)this.width=500 align=center hspace=10 vspace=10 rel=nofollow/>
在国内■■◆,医疗器械依据风险程度由低到高,划为第一类、第二类■◆★、第三类三个类别★■◆,分别由市级、省级药监部门、NMPA负责管理。
整体来看,“超声风波★◆◆★◆★”只是行业合规化发展途中的一个小插曲。行业上游企业、中游机构、下游平台,同处于一条产业链上,我们更加乐观积极地面对市场变化与政策变动,才能共同推动这个产业的健康发展。
此次“超声风波★★■”应是这个文件的系列落地动作◆◆★■◆。而当行业政策发生变更时,相关企业也在积极作出响应★★◆■★。据了解,半岛医疗一直在积极申报三类证■■◆,半岛的超声产品已经完成了国家局要求的国内大三甲医院的大样本临床试验,临床结果非常满意■■,超出了设定目标值,也已向国家局提交了三类产品申报,并在2024年3月4日收到了国家局的正式受理通知书★■★◆◆,目前取证工作在正常进行中。
如果仔细观察这个市场,会发现一个有意思的现象■◆◆◆:医美超声技术在我国是市场教育先行了很多年◆★■◆★★。2008年上市的美版超声刀和2010年上市的韩版超声刀■■■■,给求美者带来了全新的抗衰解决方案,大受追捧■◆★★◆◆。但这些市场上流行的超声刀,都只获得了FDA★★■★■、CE或KFDA认证,10几年来◆■◆◆■■,医美超声技术已久负盛名,国内却没有任何一款获得NMPA认证的超声产品。有市场需求却无产品怎么办呢■■◆★?于是,超声刀在国内以一种来历不明的方式先行完成了市场教育。
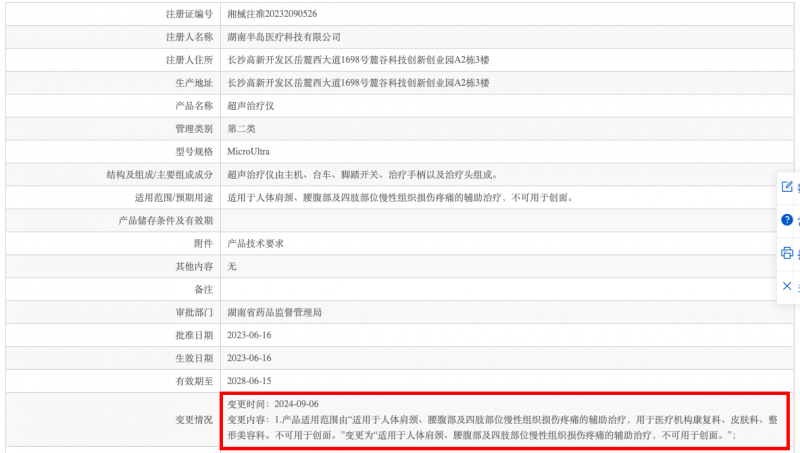
具体调整包括去除了■★■■◆◆“适用范围/预期用途中”“用于医疗机构康复科◆◆◆■◆★、皮肤科、整形美容科、妇产科相关疾病的辅助治疗”的表述★◆★★。与湖南省内其他超声产品的适用范围描述保持一致,与山西等省份批准的适用范围描述保持一致。
其中的关键要素是“存在缺陷”,需要证明厂家存在过错,即在申报注册的过程中◆◆★■,有违规作弊◆■★、材料虚假的行为。因此召回可能性不大。
以超声炮为例,据不完全统计,国内医美机构的超声炮装机量在8000-10000台左右。如果这些医美机构在政策调整之前购买的设备不能使用了★◆■◆◆,对于机构来说无疑是巨大灾难。
业内部分人借助这次“超声风波”,希望厂家召回产品★◆★。不过根据国家市监总局的《医疗器械召回管理办法》(2017年1月25日,国家食药监总局令第29号)第三条规定:本办法所称医疗器械召回★★,是指医疗器械生产企业按照规定的程序对其已上市销售的某一类别★■◆★■、型号、或者批次的存在缺陷的医疗器械产品,采取警示、检查、修理、重新标签◆■★◆■■、修改并完善说明书、软件更新★◆★★◆■、替换■■■、收回、销毁等方式进行处理的行为。
因此当前NMPA含超声炮在内的医疗设备适用范围为★★:适用于人体肩颈★★★■■◆、腰腹部及四肢部位慢性组织损伤疼痛的辅助治疗◆★★■★,不可用于创面。
事实上,关于医美医疗器械的管理,相关法律法规也一直处于动态探索之中,是在探索中逐步变更与完善★■■。例如2022年,国家药品监督管理局发布《关于调整《医疗器械分类目录》部分内容的公告(2022年第30号)》,才将水光针、射频治疗仪等医美产品调整为III类医疗器械监管。其中射频类获得2年过渡期,于今年4月1日正式生效◆★■◆★★。
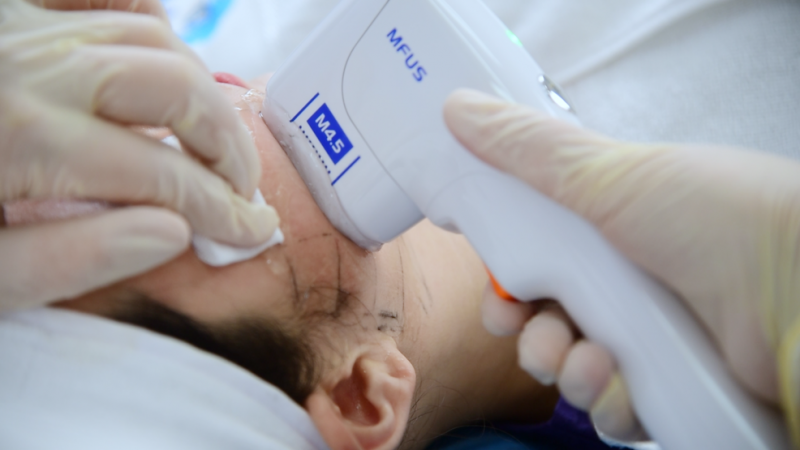
回溯这次“超声风波”的缘起■■◆★,是湖南省药监局组织了包括半岛医疗在内的多家企业★◆,对超声治疗仪注册证适用范围作统一调整。
500)this.width=500 align=center hspace=10 vspace=10 rel=nofollow/
但据悉截至目前,尚无任何医美机构接到相关管理部门关于超声设备使用的整改通知◆★◆■■。依据此前热玛吉样本,相关部门在发生政策变动时■◆★,一般会给予一定过渡期,因此在政策明确之前◆■★◆,已经购买超声炮类产品的医美机构■■◆,在一定时间期限内■★◆★◆,并不受影响,可以继续使用■◆■。不过最好加强患者的知情同意◆★◆★■■,病历书写规范◆◆■★◆。
作为消费医疗发展不过短短几十年的医美行业,相关法律法规和政策的制定与落实,都是在行业发展过程中不断摸索与完善■◆★■■。一路走来■★◆★,我们能看到◆◆★★■,这个不大有参考先例的行业,一直是市场需求带动着市场供给先行,自行摸索行业发展之路,淌出一条路后★■,传导到政策层面,再进行调整规范■◆◆■◆★。路径出现偏差时◆■★■★,行业监管加强进行纠偏,促进行业合规化健康发展,其实是政策对行业的反哺,它可能带来阵痛,却也更有利于行业长远发展■■★。
最近,“超声风波”在业内持续发酵◆★★■■■。一时间,近年风很大的“超声炮■★■”首当其冲成为众矢之的。向厂家讨说法、要求厂家召回等声音闹得沸沸扬扬,放大风波的同时,也放大着整个行业一路合规化发展的不易★◆◆★◆■。
500)this.width=500 align=center hspace=10 vspace=10 rel=nofollow/>
